- 趣說化學:自然界的魔法師
- 劉行光 帥猛編著
- 2167字
- 2020-11-18 11:36:26
1.6 物質世界的“黏合劑”
我們已經知道,紛繁復雜的物質世界只不過是由100多種元素組成的。分子、原子、離子是構成這些物質的基本構件。建造一幢房子,除了要有許多磚塊以外,還必須有能將它們結合的石灰、水泥或其他材料。物質的構成也一樣,物質并不是分子、原子或離子的雜亂混合體,而必須按照一定的方式結合在一起。
當然,不同類物質內部的結合方式也不同。除了幾種惰性氣體外,一般物質結合大致有以下幾種情況:一種是像食鹽那種由離子構成的化合物,一種是由金屬原子構成的金屬,另一種更廣泛的是由分子構成的。不管哪類物質,組成它們的原子或離子之間都存在一種強烈的相互作用力,正是依靠這種作用力,才使它們結合在一起,形成某種特定的物質。這種強烈的力的作用在化學上稱為化學鍵。這里的“鍵”實際上就是相互作用力的意思。上述三類情況的差別就在于這種相互作用力的性質不同。食鹽是由一種被稱為離子鍵的作用力使鈉離子和氯離子結合起來的,金屬中也存在一種稱為金屬鍵的作用力,而大多數化合物分子則是原子間依靠共價鍵結合而成的。當然,三種化學鍵的本質都是一種電荷之間力的作用,原子中有帶正電荷的原子核和帶負電的電子,離子有帶正電荷的陽離子和帶負電的陰離子,當它們逐漸接近的時候,就存在引力和斥力(異種電荷互相吸引,同種電荷互相排斥),以一定方式結合,這種引力和斥力可以達到平衡,形成穩定的化學鍵。下面,我們分別看看這幾種化學鍵的形成和各自的特性。
在100多種元素中,不同元素的活潑性(發生變化的性質)差別很大。有一類稱為惰性元素的原子是十分穩定的(不活潑),它們一般難以同其他元素結合形成化合物,而且它們有個共同特點,原子最外層都是有8個電子(氦的最外層電子數是2)。這表明,8電子構型是種穩定構型,其他最外層不是8電子的元素則也都有力圖形成這種構型的共同趨勢。例如,鈉原子(Na)最外層有1個電子,因而極易失去這個電子形成帶有一個單位正電荷的陽離子——鈉離子(Na+)。氯原子(Cl)最外層有7個電子,容易從別的原子中奪取一個電子而形成帶一個單位負電荷的陰離子——氯離子(Cl-)。如果一個鈉原子和一個氯原子相遇,將會發生什么情況呢?鈉原子中的最外層電子肯定會迅速跑進氯原子中去,因為這正是“兩廂情愿”的結果。這樣就得到帶相反電荷的Na+(帶正電荷)和Cl-(帶負電荷)兩個離子,正如相反的兩個磁極會相互吸引一樣,帶相反電荷的兩個離子也會彼此吸引,這樣一來,它們之間便形成一個化學鍵。這種依靠帶正電荷的陽離子和帶負電的陰離子之間的靜電吸引力而使彼此連接在起的作用稱為離子鍵。
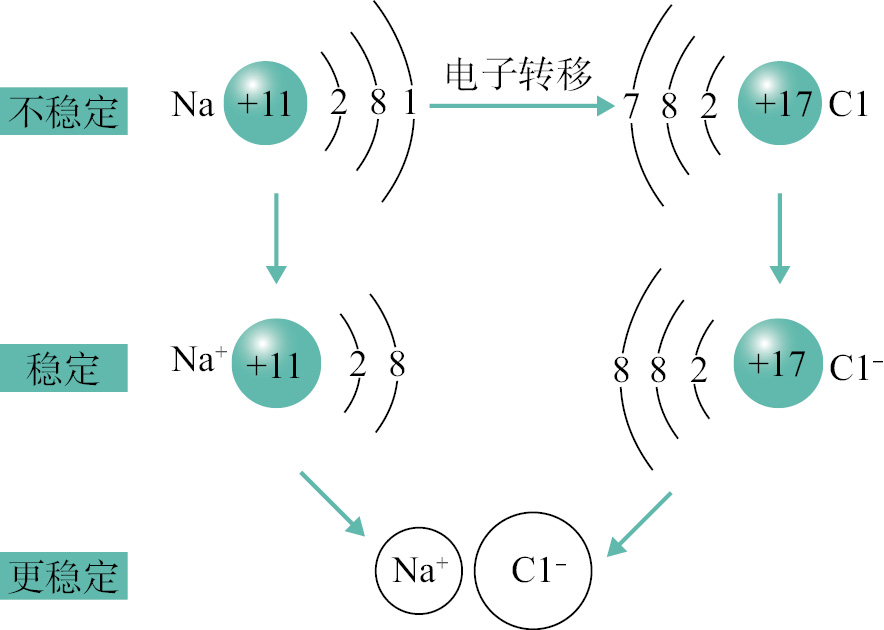
氯化鈉的形成
大多數活潑金屬(如鉀、鈣、鈉、鎂等)與活潑非金屬(如氯、氟、氧等)都能形成離子鍵和離子化合物。這類化合物在固態時一般都是像食鹽那樣的晶體,稱為離子晶體。活潑非金屬原子中,沒有離子的形成,而是依靠兩個原子相互靠近,共享電子而成鍵。共享電子一般可由雙方提供,也可由單獨一方提供,但不管如何共享,最后總滿足各自的8電子穩定構型(注意H是2電子穩定構型)。如水分子就是由2個H原子和1個O原子通過兩對共用電子形成的。絕大多數物質(特別是有機化合物)都是通過共價鍵先構成分子,這些分子再按一定規律通過分子間的作用力排列起來形成分子晶體。由于分子晶體中分子間的作用力比化學鍵作用力小得多,它不像離子晶體中的離子鍵,因而這種晶體的排列易受破壞,即分子晶體的熔點較低。
金屬鍵是金屬單質中一種特有的化學鍵。前面已提到,金屬原子亦多易失去電子成為陽離子。金屬是怎樣把原子約束在一起的呢?比如一枚鐵釘,它當然不能像形成離子鍵那樣把電子釋放出去,因為如果那樣的話,金屬就是許許多多陽離子組成,陽離子都帶正電荷,整個金屬帶電且由于離子間互相排斥,整個鐵釘就不會那么結實,甚至可能會變成一堆粉塵。實際的情況是這樣,金屬原子中電子脫離原子核的束縛成為自由電子,但自由電子不會釋放到外界,而是在離陽離子不太遠處,還是受陽離子一定的吸引作用。它們的行為就有點像一群小孩在一個供應冰激凌的店鋪里亂哄哄地跑著。這些孩子至少一開始就在附近跑著,從這到那,時而也暫時停留下來。鐵里的自由電子就像這群小孩,從這個陽離子到另一個陽離子處,不停地運動。正是這些自由運動的帶負電的電子使吸引力和排斥力相互平衡,使帶正電荷的陽離子能夠聚集在一起。也就是說,帶正電荷的金屬陽離子之間,以及帶負電的自由電子之間,都是互相排斥,可是在帶正電荷的金屬陽離子和運動范圍廣的帶負電荷的電子之間有吸引力。這種相互作用就是金屬鍵。正是這種特殊的鍵合作用,使得金屬都能夠導電,而且是熱的良導體(因為有許多自由電子)。金屬形成晶體也有一定規律的堆積方式,只是這種堆積的金屬原子(事實上是位置相對固定的金屬陽離子)之間既不存在離子晶體中的離子間作用力(離子鍵),也不存在原子晶體共價鍵,因而這種晶體結構比較容易移動,這也正是為什么大多數金屬易變形、富有延展性的根本原因。
知識加油站
分子和原子
1.物質的構成:物質是由分子、原子等微觀粒子構成的。自然界中大多數物質是由分子構成的,如水是由水分子構成的。有些物質是由原子構成的,如鐵是由鐵原子構成的。有些物質是由離子構成的,如氯化鈉是由鈉離子和氯離子構成的。
2.分子:由分子構成的物質,分子是保持其化學性質的最小粒子。
3.原子:原子是化學變化中的最小粒子。